![]() Número 27, enero, 2026:
18–44
Número 27, enero, 2026:
18–44
ISSN versión impresa: 2071–9841 ISSN versión en línea: 2079–0139 https://doi.org/10.33800/nc.vi27.387
LISTA TAXONÓMICA DE LA BIOTA MARINA ASOCIADA A LOS ESPIGONES DEL LITORAL DE TUXPAN, VERACRUZ, MÉXICO
Taxonomic checklist of the marine biota associated with the groynes of the coast of Tuxpan, Veracruz, Mexico
Vicencio de la Cruz-Francisco
Facultad de Ciencias Biológicas y Agropecuarias, Campus Tuxpan, Universidad Veracruzana. Carr. Tuxpan-
Tampico km
7.5, Col. Universitaria CP. 92854, Tuxpan, Veracruz, México.
vicenciodelacruz@gmail.com, ![]() https://orcid.org/0000-0001-8339-6730.
https://orcid.org/0000-0001-8339-6730.
[Recibido: 15 de septiembre, 2025; Aceptado: 8 de noviembre, 2025]
RESUMEN
Las estructuras de defensa costera, como los espigones de roca, proporcionan un sustrato estable para múltiples especies marinas. Sin embargo, en el litoral de Tuxpan, Veracruz, el conocimiento sobre su biodiversidad es aún limitado. Por lo tanto, el objetivo del presente estudio fue determinar la riqueza específica de la biota asociada a estos espigones. Los muestreos se realizaron durante las mareas más bajas entre 2021 y 2025, explorando las zonas altas y bajas de los espigones en áreas accesibles y seguras. En cada muestreo se registraron las especies observadas y datos de sus características morfológicas y tipo de movilidad. Se registraron tres reinos (Chromista, Plantae y Animalia), 12 filos y 124 especies marinas, además, 6 taxones solo fueron identificados a nivel familia y 15 taxones a nivel de género. El reino Animalia y el filo Mollusca presentaron la mayor riqueza específica. Se distinguió una zonación vertical, registrándose mayor número de especies en las zonas bajas y pozas de marea en comparación con las zonas altas. Se adicionan cuatro nuevos registros para el suroeste del golfo de México, y se confirma la presencia de dos especies exóticas en la zona norte de Veracruz. Los resultados obtenidos constituyen un gran avance al conocimiento de la biodiversidad marina para estas estructuras artificiales, sin embargo, es necesario más investigaciones que contribuyan a reducir vacíos de conocimiento en diversos grupos de invertebrados. La presente información puede apoyar el desarrollo de estrategias de manejo, conservación, así como actividades dirigidas a la detección y monitoreo de especies exóticas.
Palabras clave: algas marinas, invertebrados marinos, zonación, intermareal.
ABSTRACT
Coastal defense structures, such as rock groynes, provide a stable substrate for multiple marine species. However, in the coastal zone of Tuxpan, Veracruz, knowledge of their associated biodiversity remains limited. Therefore, the objective of this study was to determine the specific richness of the biota associated with these groynes. Sampling was conducted during the lowest tides between 2021 and 2025, exploring the upper and lower zones of the groynes in accessible and safe areas. During each sampling event, observed species were recorded, along with data on their morphological characteristics and type of mobility. A total of three kingdoms (Chromista, Plantae and Animalia), 12 phyla, and 124 marine species were recorded. Additionally, six taxa were identified only to the family level and 15 taxa to the genus level. The kingdom Animalia and the phylum Mollusca exhibited the highest species richness. A clear vertical zonation was observed, with a higher number of species in the lower zones and tidal pools compared to the upper zones. Four new records are added for the southwestern Gulf of Mexico, and the presence of two exotic species in the northern Veracruz is confirmed. These results represent a significant advancement in the understanding of marine biodiversity associated with these artificial structures. However, further research is needed to help reduce knowledge gaps; however, further research is needed to help reduce knowledge gaps in various invertebrate groups. The information presented here may support the development of management an conservation strategies, as well as activities aimed at the detection and monitoring of exotic species.
Keyworks: seaweed, marine invertebrates, zonation, intertidal.
INTRODUCCIÓN
Los ecosistemas costeros y marinos de Tuxpan, Veracruz, incluyen principalmente manglares, una laguna costera, el río Tuxpan, pastos marinos, arrecifes coralinos y un litoral arenoso de pendiente suave (López-Portillo et al., 2023; Ortiz-Lozano et al., 2010). Estos ecosistemas naturales han sido objeto de numerosos estudios que han documentado su biodiversidad marina, principalmente en los arrecifes coralinos y la laguna de Tampamachoco. En estos ecosistemas se tiene conocimiento de la flora marina bentónica (De la Cruz-Francisco et al., 2020; Dreckmann & Pérez-Hernández, 1994; García-López et al., 2017; Mateo-Cid et al., 2024), zooplancton (Flores-Galicia & De la Cruz-Francisco, 2018; López-Torres et al., 2023; Román-Hernández et al., 2006), así como de diversos grupos de invertebrados, incluyendo esponjas (De la CruzFrancisco et al., 2016a), anémonas (De la Cruz-Francisco & González-Muñoz, 2019), corales y octocorales (De la Cruz-Francisco et al., 2016b), moluscos (De la Cruz-Francisco et al., 2017c; De la Cruz-Francisco et al., 2023; De la Cruz-Francisco & González-Gándara, 2006; Reguero et al., 1991), crustáceos (Hermoso-Salazar et al., 2019; Hernández et al., 2010), equinodermos (De la Cruz-Francisco et al., 2017a; González-Gándara et al., 2015b; Morales-Quijano et al., 2017) y peces (González-Gándara et al., 2012).
El litoral de Tuxpan es predominantemente arenoso, presenta en su zona turística estructuras artificiales de protección como los espigones, cuya función es controlar la erosión de la costa y atenuar la fuerza del oleaje. Además, en la desembocadura del río Tuxpan se han establecido dos escolleras que facilitan la entrada y salida del tránsito marítimo (López-Portillo et al., 2023). Estas estructuras se encuentran sumergidas parcialmente en el litoral, por lo tanto, proporcionan un sustrato sólido que sirve como hábitat para el asentamiento de diversos organismos marinos. Se ha documentado que estos hábitats artificiales permiten el desarrollo de comunidades biológicas integradas por algas, esponjas, hidroides, balanos, moluscos, briozoos, crustáceos, equinodermos y peces (Bulleri & Chapman, 2004; Firth et al., 2013; Hall et al., 2018; Masi et al., 2009). Sin embargo, también se ha señalado que los espigones y otras estructuras de defensa costera pueden favorecer el asentamiento y dispersión de especies exóticas e invasoras (Mineur et al., 2012; Vaselli et al., 2008).
A pesar de la accesibilidad de estas estructuras artificiales en el litoral de Tuxpan, el conocimiento sobre su biodiversidad sigue siendo limitado en comparación con los ecosistemas naturales aledaños. Entre los grupos estudiados se encuentran las algas marinas bentónicas (García-López et al., 2017; Mateo-Cid et al., 2024) y picnogónidos con registros específicos para las escolleras (Child, 1992). Recientemente, se ha documentado la presencia de esponjas (De la Cruz-Francisco, 2025a) y babosas marinas en los espigones (De la Cruz-Francisco, 2025b), así como también, se ha reportado la presencia de un bivalvo exótico (Electroma vexilum) que se desarrolla sobre algas bentónicas nativas (De la Cruz-Francisco, 2025c). Si bien, estos estudios confirman la presencia de organismos asociados a estas estructuras, incluyendo una especie exótica, la composición de otros grupos de algas bentónicas, invertebrados y peces aún se desconoce en esta localidad.
Por lo anterior, el presente trabajo determinó la riqueza específica de las especies marinas asociadas a los espigones de Tuxpan, Veracruz, con información de su distribución vertical y atributos morfológicos, incluyendo nuevos registros para la región y el reporte de especies exóticas. Aunque se trata de una lista preliminar, este trabajo contribuye al conocimiento de la biodiversidad marina asociada a hábitats artificiales en el sur del golfo de México, y sienta las bases para futuras investigaciones más detalladas sobre estos ambientes artificiales.
OBJETIVOS
- Documentar la composición de la biota marina asociada a los espigones del litoral de Tuxpan, Veracruz, mediante una lista taxonómica y la caracterización de su distribución vertical y atributos morfológicos.
MATERIALES Y MÉTODOS
Área de estudio. El municipio de Tuxpan se localiza en el norte del estado de Veracruz, al suroeste del golfo de México, y presenta un litoral arenoso con pendiente suave. Esta localidad tiene relevancia turística y destaca el transito marítimo nacional e internacional, ya que presenta un puerto marítimo industrial y comercial (Fig. 1A). A lo largo de la franja costera se encuentran 35 localidades, siendo Barra Norte, San Antonio y Villamar Chile Frio las comunidades rurales más cercanas a la costa. En la zona turística de playa San Antonio, se localizan 16 espigones construidos en 2016 con roca basáltica, ubicadas dentro de la zona intermareal. Estas estructuras de protección son rectas y cortas (aproximadamente 60 m de longitud), con una cresta emergente y están posicionadas de forma perpendicular al litoral, con una separación promedio de 160 m entre uno y otro espigón (Fig. 1B-D). Los espigones se ubican a lo largo de un tramo de 2 km del litoral de Tuxpan; al norte colindan con la Central Termoeléctrica “Adolfo López Mateos”, mientras que, al sur, a una distancia de 2.46 km se encuentra la desembocadura del rio Tuxpan, la cual posee dos escolleras de aproximadamente 1 km de longitud (López-Portillo et al., 2023).
El litoral de Tuxpan tiene influencia de la descarga del río Tuxpan, principalmente durante las precipitaciones (Salas-Pérez et al., 2015) y presenta a lo largo del año cambios estacionales en la temperatura del agua al igual que en la dinámica de las corrientes marinas. Durante los meses de otoño (septiembre-diciembre) e invierno (diciembre-marzo), las temperaturas del agua descienden (22–23 °C) y las corrientes marinas superficiales se desplazan de norte a sur, impulsados por vientos conocidos localmente como “nortes”, los cuales alcanzan velocidades de hasta 140 km/h. Mientras, en las estaciones de primavera (marzo-junio) y verano (junioseptiembre) las aguas se vuelven más cálidas (27–28 °C) y las corrientes cambian su dirección, moviéndose de sur a norte, lo cual está asociado al cambio de la dirección del viento conocidos localmente como suradas que alcanzan velocidades de hasta 80 km/h (Mendelssohn et al., 2017; Ortiz-Lozano et al., 2010; Zavala-Hidalgo et al., 2003). Un tercer patrón de corrientes ocurre durante la transición de nortes a suradas, cuando los vientos dominantes son en dirección esteoeste, generando corrientes superficiales perpendiculares cercanas a la costa a los 20° de la latitud norte, y al llegar al norte de Tecolutla incluyendo Tuxpan, estas corrientes se vuelven paralelas y se desplazan en dirección norte rumbo a Tampico, Tamaulipas (Ortiz-Lozano et al., 2010).
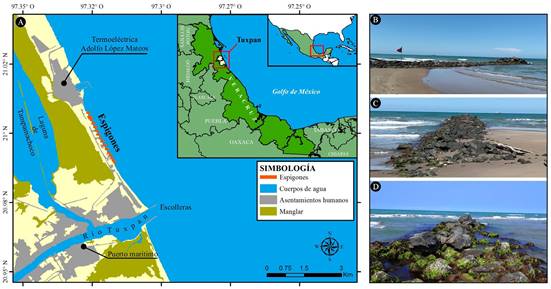
Figura 1. Zona central del litoral de Tuxpan, Veracruz. A, localización geográfica de los espigones; B, perfil lateral de un espigón; C, parte posterior de un espigón; D, frente de un espigón.
Muestreo e identificación de especies. Los muestreos se realizaron entre el 2021 y 2025, durante las mareas más bajas registradas en los meses de enero, febrero, junio y julio. Dado que los espigones se encuentran instalados en la zona intermareal y presentan una pendiente suave, los muestreos se realizaron en dos zonas. Zona alta, corresponde a la parte posterior del espigón, generalmente expuesta a la radiación solar, desecación y viento. Zona baja, se localiza en la parte frontal del espigón, recibe el embate directo del oleaje; generalmente esta zona queda cubierta y descubierta por el ascenso y descenso de las mareas. Esta zona presenta mayor diversidad y abundancia de organismos marinos. En la zona baja, también se registró información en las pozas de marea, donde generalmente suelen encontrarse organismos móviles como decápodos y peces (Fig. 1C-D).
Los recorridos se efectuaron sobre la cresta y los costados de los espigones, especialmente en áreas accesibles y seguras para evitar accidentes, iniciando el recorrido desde la parte posterior (zona alta) hacia el frente del espigón (zona baja). En cada recorrido se revisó la superficie de las rocas, las oquedades y las pozas de marea (Fig. 1B-D), así como las frondas de macroalgas para recolectar algas epifitas y organismos epibiontes. Los ejemplares fueron recolectados manualmente y apoyándose de una espátula, navaja y pinzas de disección. Las algas bentónicas fueron fijadas en formol al 5% diluido con agua de mar, mientras que los invertebrados se conservaron en alcohol etílico al 70%. Todo el material colectado se depositó en la colección biológica de la Facultad de Ciencias Biológicas, de la Universidad Veracruzana, campus Tuxpan.
La mayoría de los ejemplares fueron identificados a nivel especie y en algunos casos se identificaron a nivel género o familia, utilizando guías y claves de identificación para los distintos grupos biológicos: macroalgas (Dreckman, 2012; León-Álvarez et al., 2007; Littler & Littler, 2000; Mendoza-González et al., 2014; Miranda-Alves et al., 2009; Pacheco-Cervera et al., 2010; Quiroz-González et al., 2017), esponjas (Díaz et al., 1993; van Soest, 2017; Zea & De Weerdt, 1999), cnidarios (Colín-García et al., 2018; De la Cruz-Francisco & GonzálezMuñoz, 2019), anélidos (Chávez-López, 2020), moluscos (García-Cubas y Reguero, 2004; 2007), picnogónidos (Child, 1992), crustáceos (Abele y Kim, 1986; Celis et al., 2007), briozoos (Vieira et al., 2016; Winston, 1982), equinodermos (Borrero et al., 2012), ascidias (Oliveira et al., 2014) y peces (Humman y Deloach, 2002). Con las especies identificadas, se elaboró una lista taxonómica agrupado por Reino, Filo, Clase y Orden de forma filogenética, mientras las categorías de Familia, Género y Especie se ordenaron alfabéticamente.
La lista de especies fue complementada con datos de la zonación vertical, especificando la presencia de las especies en la zona alta y/o baja de los espigones, incluyendo las pozas de marea. También, se incluyeron atributos morfológicos, para el caso de las algas bentónicas se registraron datos de la forma de vida, el tipo de talo y eje de crecimiento (León-Álvarez et al., 2007). Respecto a la fauna bentónica, se recabaron datos del tipo de movilidad considerando tres categorías: sésil (fijados al sustrato), sedentario (movilidad lenta/restringida) y vágil (alta movilidad). A su vez, los organismos sésiles coloniales fueron clasificados según su forma de crecimiento: incrustante, masiva, hemisférica y arborescente. Finalmente, el inventario taxonómico de los espigones se complementó con referencias bibliográficas para confirmar la presencia de las especies en el litoral de Tuxpan y el litoral de Veracruz, así también para identificar nuevos registros, los cuales corresponden a las especies que carecen de registros previos en la literatura consultada para la región.
RESULTADOS
En este estudio se identificaron un total de 124 taxones a nivel de especie, distribuidos en tres reinos y 12 filos. El reino Animal fue el más representativo, con ocho filos y 80 especies, mientras que las algas marinas están representadas por 43 especies, también se registró un Chromista no fotosintético del filo Foraminífera (Fig. 2) identificado como Homotrema rubrum (Fig. 3E). Adicionalmente, se registra por primera vez para la zona norte de Veracruz al poliqueto Phragmatopoma caudata (Fig. 3N), mientras, el hidrozoo Pennaria disticha (Fig. 3F), los briozoos Licornia cf. regularis y Biflustra cf. savartii (Fig. 3E) y el picnógonido Ammothella appendiculata (Fig. 3K), constituyen nuevos registros para el suroeste del golfo de México. Así mismo, se confirma la presencia del coral exótico Oculina patagonica (Fig. 3H) y del bivalvo Electroma vexillum (Fig. 3J) (Tabla I).
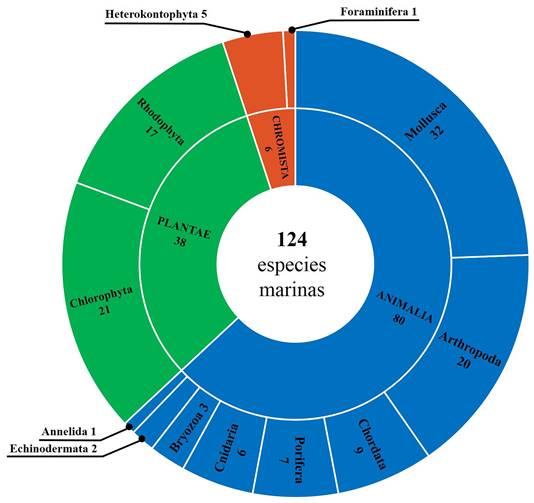
Figura 2. Número de taxones por Reino y Filo identificados a nivel de especie asociados en los espigones de Tuxpan, Veracruz.
Las algas marinas bentónicas identificadas en los espigones pertenecen a los grupos Heterokontophyta, Rhodophyta y Chlorophyta, este último grupo fue el de mayor riqueza, con 21 especies, seguido por Rhodophyta con 17 especies (incluyendo tres taxones identificados a nivel género). En Heterokontophyta, se identificaron cinco especies y dos taxones a nivel de género (Tabla I; Fig. 2). A nivel de Orden, Bryopsidales y Cladophorales fueron los que presentaron siete y ocho especies, respectivamente. La mayoría de las macroalgas registradas en los espigones fueron epilíticas y de crecimiento erecto, con talos principalmente arbustiformes y filamentosos. Algunas especies presentaron formas postradas como Colpomenia sinuosa (Fig.
3A) y formas estoloníferas como Caulerpa racemosa (Fig. 3B) y Caulerpa mexicana (Fig. 3C).
Con relación a la distribución vertical, la riqueza ficológica fue mayor en las zonas bajas de los espigones registrándose 47 especies, seguido de las pozas de marea con 28 especies (Fig. 4). En los costados de los espigones de la zona baja se observaron amplios matorrales de algas rojas representadas principalmente por especies del género Acantophora, Alsidium, Hypnea y Gracilaria. Por el contrario, en las partes altas se registraron únicamente nueves especies representadas por algas verdes de los géneros Chaetomorpha, Cladophora y Ulva (Fig. 4).
En cuanto a la fauna marina, a nivel de Filo, Mollusca y Arthropoda fueron los grupos más diversos, con 32 y 20 especies respectivamente (Fig. 2). A nivel de Orden, Decapoda fue el más representativo con 13 especies y tres géneros identificados (Tabla II). De igual manera, la distribución vertical de la fauna marina presentó su mayor riqueza en la zona baja con 79 especies, siendo moluscos y artrópodos los más representativos con 33 y 20 especies, respectivamente. En cambio, en las pozas de marea se registraron 28 especies, y en la zona alta solo se identificaron 20 taxones (Fig. 4). Mientras, 18 especies representados por gasterópodos, balanos y crustáceos decápodos fueron comunes de observar en la zona alta y baja de los espigones (Tabla II).
Respecto a la movilidad, la fauna vágil fue la de mayor representación con 61 taxones que en su mayoría correspondieron a gasterópodos, picnogónidos, crustáceos, equinodermos y peces. Estos organismos fueron observados principalmente en la zona baja de los espigones. No obstante, gasterópodos como Nerita, Echinolittorina, Stramonita (Fig. 3J) y el equinodermo como Echinometra lucunter y Holothuria (Halodeima) grisea (Fig. 3P) se encontraron tanto en la zona alta y baja. En cambio, poliquetos, crustáceos decápodos, picnogónidos y peces se localizaron en la zona baja y pozas de marea asociados a macroalgas e hidrozoos arborescentes (Tabla II). Entre las especies más comunes de este grupo fueron Acanthonyx pettiverii
(Fig. 3M), Eriphia gonagra, Grapsus grapsus, Halichoeres bivittatus y Abudefduf saxatilis (Fig. 3R). Respecto a la fauna sedentaria, presentó una menor riqueza específica y entre las especies observadas fueron Bunodosoma cavernatum y Actinostella flosculifera (Fig. 3G)
Por último, la fauna sésil fue la menos diversa en taxones, siendo las formas coloniales incrustantes las más comunes como Placospongia ruetzleri (Fig. 3D) y Didemnum sp. (Fig. 3Q), representadas principalmente por esponjas (cinco taxones) y ascidias (tres taxones), localizadas en la zona baja y en las pozas de marea. En cuanto a los organismos unitarios sésiles como los balanos Chthamalus fragilis (Fig. 3J) y Tetraclita stalactifera (Fig. 3L), fueron más frecuentes en la zona alta, aunque también se encontraron en menor frecuencia en la parte baja de los espigones.

Figura 3. Especies marinas que habitan en los espigones de Tuxpan, Veracruz, México. A, Colpomenia sinuosa; B, Caulerpa racemosa; C, Caulerpa mexicana; D, Placospongia ruetzleri; E, Biflustra cf. savartii (incrustación blanca) y Homotrema rubrum; F, Pennaria disticha; G, Actinostella flosculifera; H, Oculina patagonica; I, Electroma vexillum; J, Stramonita floridana y Chthamalus fragilis; K, Ammothella appendiculata; L, Tetraclita stalactifera; M, Acanthonyx petiverii; N, Phragmatopoma caudata; O, Thalamoporella floridana; P, Holothuria (Halodeima) grisea y Echinometra lucunter; Q, Didemnum sp.; R, Halichoeres bivittatus y Abudefduf saxatilis.
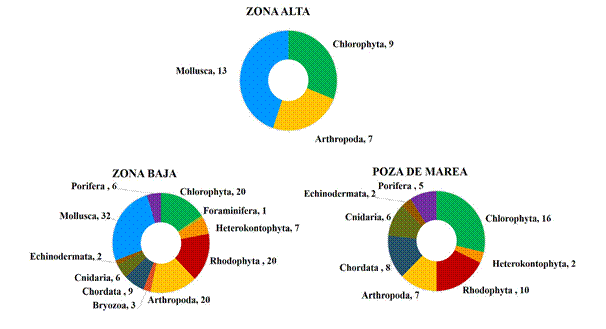
Figura 4. Número de taxones por Filo identificados a nivel de especie registrados en la zona alta, zona baja y pozas de marea en los espigones de Tuxpan, Veracruz.
|
Categorías taxonómicas REINO CHROMISTA FILO FORAMINIFERA Clase Globothalamea Orden Rotallida |
FV |
EC |
FT |
Zonación |
Espigones y referencias en el litoral de Tuxpan |
Referencias en litoral de Veracruz |
|
Homotrema rubrum (Lamarck, 1816) FILO HETEROKONTOPHYTA Clase Phaeophyceae Orden Dictyotales |
incr |
|
|
ZB |
● |
|
|
Dictyota sp. |
epil |
ere |
aci |
ZB, PM |
● |
|
|
Padina sp. |
epil |
ere |
flab |
ZB |
● |
|
![]() Tabla I. Lista de especies bentónicas
de los reinos Chromista (foraminíferos y algas pardas) y Plantae (algas rojas y
verdes) registradas en los espigones del litoral de Tuxpan, Veracruz, México
(●). Abreviaciones. Forma de vida (FV): epilítico (epil), epifítica
(epif). Eje de crecimiento (EC): erecto (ere), postrado (post). Forma del talo
(FT): acintado (aci), arbustiforme (arb), estolonífero (est), filamentoso
(fil), flabelado (flab), globoso (glob), lamina (lam). Zonación vertical de las
especies en los espigones: zona alta (ZA), zona baja (ZB), poza de marea (PM).
Tabla I. Lista de especies bentónicas
de los reinos Chromista (foraminíferos y algas pardas) y Plantae (algas rojas y
verdes) registradas en los espigones del litoral de Tuxpan, Veracruz, México
(●). Abreviaciones. Forma de vida (FV): epilítico (epil), epifítica
(epif). Eje de crecimiento (EC): erecto (ere), postrado (post). Forma del talo
(FT): acintado (aci), arbustiforme (arb), estolonífero (est), filamentoso
(fil), flabelado (flab), globoso (glob), lamina (lam). Zonación vertical de las
especies en los espigones: zona alta (ZA), zona baja (ZB), poza de marea (PM).
![]()
Orden Sphacelariales
|
Categorías taxonómicas |
FV EC |
FT |
Zonación |
Espigones y referencias en el litoral de Tuxpan |
Referencias en litoral de Veracruz |
|
|
Sphacelaria rigidula Kützing |
epil, ere epif |
fil |
ZB |
● |
J |
|
|
Sphacelaria tribuloides Meneghini Orden Ectocarpales |
epil, ere |
fil |
ZB |
● |
J |
|
|
epif |
|
|||||
|
Chnoospora minima (Hering) Papenfuss |
epil |
ere |
arb |
ZB, PM |
● |
B, F, H, J |
|
Colpomenia sinuosa (Mertens ex Roth) Derbès & Solier |
epil |
post |
glob |
ZB |
● |
B, E, F, H, J |
|
Feldmannia mitchelliae (Harvey) H.-S.Kim REINO PLANTAE FILO RHODOPHYTA Clase Florideophyceae Orden Corallinales |
epif |
|
fil |
ZB |
● |
J |
|
Amphiroa fragilissima (Linnaeus) J.V.Lamouroux |
epil |
ere |
arb |
ZB, PM |
● |
I |
|
Jania capillacea Harvey |
epil |
ere |
arb |
ZB, PM |
● |
J |
|
Jania rubens (Linnaeus) J.V.Lamouroux Orden Ceramiales |
epil |
ere |
arb |
ZB, PM |
● |
B, C, F, J |
|
Acanthophora spicifera (M. Vahl) Börgesen |
epil |
ere |
arb |
ZB, PM |
● |
C, E, F, G, I, J |
|
Alsidium triquetrum (S.G.Gmelin) Trevisan |
epil |
ere |
arb |
ZB |
● |
B, C, E, F, G, I, J |
|
Centroceras clavulatum (C.Agardh) Montagne |
epif |
ere |
fil |
ZB, PM |
● |
C, E, F, G, I |
|
Ceramium cimbricum H.E.Petersen |
epif |
ere |
fil |
ZB, PM |
● |
E, J |
|
Laurencia sp. |
epil |
ere |
arb |
ZB |
● |
|
|
Polysiphonia sp. |
epil |
ere |
arb |
ZB |
● |
|
|
Spyridia filamentosa (Wulfen) Harvey Orden Gigartinales |
epil |
ere |
arb |
ZB |
● |
G, J |
|
Agardhiella subulata (C.Agardh) Kraft & M.J.Wynne |
epil |
ere |
arb |
ZB |
●, J |
A, G, H |
|
Hypnea musciformis (Wulfen) J.V.Lamouroux |
epil |
ere |
arb |
ZB, PM |
●, J |
A, B, C, E, F, G, I, J |
|
Hypnea spinella (C.Agardh) Kützing |
epil |
ere |
arb |
ZB, PM |
● |
B, C, E, F, G, I, J |
|
Solieria filiformis (Kützing) P.W.Gabrielson Orden Gracilariales |
epil |
ere |
arb |
ZB |
●, J |
J |
|
Gracilaria blodgettii Harvey |
epil |
ere |
arb |
ZB, PM |
● |
C, E, F, G, J |
|
Gracilaria damicornis J.Agardh |
epil |
ere |
arb |
ZB |
● |
A, C, E, G, J |
|
Gracilaria domingensis (Kützing) Sonder ex Dickie |
epil |
ere |
arb |
ZB |
●, J |
B, E, J |
|
Gracilaria flabelliformis (P.Crouan & H.Crouan) Fredericq & Gurgel |
epil |
ere |
arb |
PM |
●, J |
F, J |
![]() Cont. Tabla I
Cont. Tabla I
Cont. Tabla I
|
Categorías taxonómicas |
FV |
EC |
FT |
Zonación |
Espigones y referencias en el litoral de Tuxpan |
Referencias en litoral de Veracruz |
|
Gracilariopsis lemaneiformis (Bory) E.Y.Dawson, Acleto & Foldvik |
epil |
ere |
arb |
ZB, PM |
● |
E, J |
|
Orden Halymeniales Grateloupia sp. |
epil |
ere |
arb |
ZB |
● |
|
|
FILO CHLOROPHYTA Clase Ulvophyceae Orden Bryopsidales Bryopsis hypnoides J.V.Lamouroux |
epil |
ere |
fil |
ZB, PM |
●, D, J |
D, J |
|
Bryopsis pennata J.V.Lamouroux, |
epil |
ere |
fil |
ZB, PM |
●, J |
B, D, E, F, J |
|
Caulerpa chemnitzia (Esper) J.V.Lamouroux |
epil |
ere |
est |
ZB, PM |
●, D, J |
D, F, J |
|
Caulerpa mexicana Sonder ex Kützing |
epil |
ere |
est |
ZB, PM |
●, D, J |
C, D, E, I, J |
|
Caulerpa microphysa (Weber Bosse) Feldmann |
epil |
ere |
est |
ZB, PM |
● |
D, F, J |
|
Caulerpa racemosa (Forsskål) J.Agardh |
epil |
ere |
est |
ZB, PM |
●, J |
B, C, D, E, F, I, J |
|
Caulerpa sertularioides (S.G.Gmelin) M.Howe |
epil |
ere |
est |
ZB, PM |
●, D, J |
B, D, E, F, I, J |
|
Orden Cladophorales Chaetomorpha aerea (Dillwyn) Kützing |
epil |
ere |
fil |
ZA, ZB, PM |
● |
B, C, D, E, F, I, J |
|
Chaetomorpha antennina (Bory) Kützing |
epil |
ere |
fil |
ZB, PM |
●, D, J |
C, D, E, F, J |
|
Chaetomorpha gracilis Kützing |
epil |
ere |
fil |
ZA, ZB |
● |
C, D, J |
|
Cladophora prolifera (Roth) Kützing |
epil |
ere |
fil |
ZA, ZB |
● |
C, D, E, F, J |
|
Cladophora vagabunda (Linnaeus) Hoek |
epil |
ere |
fil |
ZA, ZB, PM |
●, D, J |
A, C, D, E, F, I, J |
|
Cladophoropsis macromeres W.R.Taylor |
epil |
ere |
fil |
ZB, PM |
● |
J |
|
Cladophoropsis membranacea (Bang ex C.Agardh) Børgesen |
epil |
ere |
fil |
PM |
● |
J |
|
Rhizoclonium riparium (Roth) Harvey |
epil |
ere |
fil |
ZA, ZB, PM |
●, J |
B, D, F |
|
Orden Ulvales Ulva compressa Linnaeus |
epil |
ere |
fil |
ZA, ZB |
●, D |
D, J |
|
Ulva flexuosa Wulfen |
epil |
ere |
lam |
ZA, ZB |
●, J |
B, C, D, E, F, I, J |
|
Ulva intestinalis Linnaeus |
epil |
ere |
fil |
ZA, ZB |
● |
D, J |
|
Ulva lactuca Linnaeus |
epil |
ere |
lam |
ZA, ZB, PM |
●, D, J |
A, B, C, D, I, J |
|
Ulva prolifera O.F.Müller |
epil |
ere |
fil |
ZA, ZB |
●, D, J |
D, J |
|
Ulva rigida C.Agardh |
epil |
ere |
lam |
ZA, ZB |
●, J |
D, E, F, J |
Referencias: A= Huerta-Múzquiz (1960). B= Sánchez-Rodríguez (1980). C= De la Cruz-Francisco et al. (2017b). D= García-López et al. (2017). E= Arvizu-Coyotzi (2019). F= Landa-Cansigno et al. (2019); G= García-García et al. (2020). H= García-García et al. (2021). I= Rodríguez-Muñoz et al. (2023). J= Mateo-Cid et al. (2024).
Tabla II. Lista actualizada de la macrofauna bentónica registradas en este estudio para los rompeolas del litoral de Tuxpan, Veracruz, México (●). Abreviaciones. Forma de la colonia para organismos modulares (FC): masivo (masi), incrustante (incr), hemisférico (hemi), arborescente (arbo). Tipo de movilidad (MO): sésil (ses), sedentario (sed), vágil (vag). Zonación vertical de las especies en los espigones: zona alta (ZA), zona baja (ZB), poza de marea (PM).
![]()
|
Categorías taxonómicas
REINO ANIMALIA FILO PORIFERA Clase Demospongiae Orden Axinellida |
FC/MO
|
Zonación
|
Espigones y referencias en el litoral de Tuxpan
|
Referencias en litoral de Veracruz
|
|
Cyamon vickersii (Bowerbank, 1864) Orden Clionaida |
incr |
ZB, PM |
●, M |
|
|
Placospongia ruetzleri Van Soest, 2017 Orden Suberitida |
incr |
ZB, PM |
●, M |
|
|
Hymeniacidon heliophila (Wilson, 1911) |
incr |
ZB, PM |
●, M |
|
|
Suberites aurantiacus (Duchassaing & Michelotti, 1864) Orden Haplosclerida |
masi |
PM |
●, M |
|
|
Haliclona (Haliclona) epiphytica Zea & de Weerdt, 1999 Orden Tethyida |
masi |
ZB |
●, M |
|
|
Timea hechteli Lehnert & Heimler, 2001 Orden Poecilosclerida |
incr |
ZB |
●, M |
|
|
Clathria sp. Orden Tetractinellida |
incr |
ZB |
●, M |
|
|
Cinachyrella alloclada (Uliczka, 1929) FILO CNIDARIA Clase Hydrozoa Orden Anthoathecata |
hemi |
ZB, PM |
●, M |
I, L |
|
Pennaria disticha Goldfuss, 1820 Orden Leptothecata |
arbo |
ZB, PM |
● |
|
|
Macrorhynchia sp. Clase Antozoa Orden Actiniaria |
arbo |
ZB, PM |
● |
|
|
Actinostella flosculifera (Le Sueur, 1817) |
sed |
ZB, PM |
● |
H, I, L |
|
Anemonia sargassensis Hargitt, 1908 |
sed |
ZB, PM |
● |
L |
|
Bunodosoma cavernatum (Bosc, 1802) |
sed |
ZB, PM |
● |
I, L |
|
Exaiptasia diaphana (Rapp, 1829) Orden Scleractinia |
sed |
ZB, PM |
● |
L |
|
Oculina patagonica de Angelis D’Ossat, 1908 [exótica] |
incr |
ZB, PM |
● |
I, L |
|
Categorías taxonómicas FILO MOLLUSCA Clase Bivalvia Orden Mytilida |
FC/MO |
Zonación |
Espigones y referencias en el litoral de Tuxpan |
Referencias en litoral de Veracruz |
|
Brachidontes exustus (Linnaeus, 1758) Orden Ostreida |
ses |
ZB |
● |
A, H, I |
|
Electroma vexillum (Reeve, 1857) [exótica] |
ses |
ZB |
●, O |
|
|
Isognomon bicolor (C. B. Adams, 1845) |
ses |
ZB |
● |
A, L |
|
Isognomon radiatus (Anton, 1838) Orden Venerida |
ses |
ZB |
● |
A, H, I |
|
Chama macerophylla Gmelin, 1791 Clase Gastropoda Orden Lepetellida |
ses |
ZB |
● |
A |
|
Fissurella barbadensis (Gmelin, 1791) |
sed |
ZA, ZB |
● |
A |
|
Fissurella rosea (Gmelin, 1791) Orden Trochida |
sed |
ZA, ZB |
● |
|
|
Eulithidium adamsi (R. A. Philippi, 1853) Orden Cycloneritida |
vag |
ZB |
● |
I |
|
Nerita fulgurans Gmelin, 1791 |
vag |
ZA, ZB |
● |
A, I |
|
Nerita tessellata Gmelin, 1791 |
vag |
ZA, ZB |
● |
A, H, I, L |
|
Nerita versicolor Gmelin, 1791 |
vag |
ZA, ZB |
● |
A |
|
Nerita peloronta Linnaeus, 1758 Orden Caneogastropoda |
vag |
ZA, ZB |
● |
|
|
Epitonium sp. |
vag |
ZB |
● |
|
|
Hinea lineata (da Costa, 1778) |
vag |
ZB |
● |
A, H, I, |
|
Marshallora nigrocincta (C. B. Adams, 1839) Orden Littorinimorpha |
vag |
ZB |
● |
|
|
Dendropoma corrodens (A. d’Orbigny, 1841) |
ses |
ZB |
● |
I |
|
Echinolittorina angustior (Mörch, 1876) |
vag |
ZA, ZB |
● |
I, L |
|
Echinolittorina meleagris (Potiez & Michaud, 1838) |
vag |
ZA, ZB |
● |
A, I |
|
Echinolittorina ziczac (Gmelin, 1791) |
vag |
ZA, ZB |
● |
A, I |
|
Petaloconchus varians (A. d’Orbigny, 1839) Orden Neogastropoda |
ses |
ZB |
● |
A, H, I |
|
Leucozonia nassa (Gmelin, 1791) |
vag |
ZB |
● |
A, H, I, L |
|
Mitrella ocellata (Gmelin, 1791) |
vag |
ZB |
● |
A, H, I |
|
Parvanachis obesa (C. B. Adams, 1845) |
vag |
ZB |
● |
I |
|
Plicopurpura patula (Linnaeus, 1758) |
vag |
ZB |
● |
A |
|
Stramonita haemastoma (Linnaeus, 1767) |
vag |
ZA, ZB |
● |
A |
|
Categorías taxonómicas |
FC/MO |
Zonación |
Espigones y referencias en el litoral de Tuxpan |
Referencias en litoral de Veracruz |
|
Stramonita rustica (Lamarck, 1822) Orden Cephalaspidea |
vag |
ZA, ZB |
● |
H, I, L |
|
Bulla occidentalis A. Adams, 1850 Superorden Sacoglossa |
vag |
ZB |
● |
A, H, I, L |
|
Oxynoe antillarum Mörch, 1863 |
vag |
ZB |
●, N |
I, L |
|
Calliphylla mediterranea A. Costa, 1867 Orden Nudibranchia |
vag |
ZB |
●, N |
|
|
Spurilla braziliana MacFarland, 1909 |
vag |
ZB |
●, N |
|
|
Learchis poica Ev. Marcus & Er. Marcus, 1960 |
vag |
ZB |
●, N |
|
|
Phidiana lynceus Bergh, 1867 Orden Siphonariida |
vag |
ZB |
●, N |
I, L |
|
Siphonaria pectinata (Linnaeus, 1758) FILO ANNELIDA Clase Polychaeta Orden Phyllodocida |
sed |
ZA, ZB |
● |
A, I, L |
|
Nereididae |
vag |
ZB |
● |
|
|
Phyllodocidae |
vag |
ZB |
● |
|
|
Polynoidae Orden Terebellida |
vag |
ZB |
● |
|
|
Terebellidae Infraclase Canalipalpata |
vag |
ZB |
● |
|
|
Phragmatopoma caudata Krøyer in Mörch, 1863 FILO ARTHROPODA Clase Pycnogonida Orden Pantopoda |
vag |
ZA, ZB |
● |
K |
|
Ammothella appendiculata Dohrn, 1881 |
vag |
ZB |
● |
|
|
Anoplodactylus californicus Hall, 1912 |
vag |
ZB |
● |
C, E |
|
Endeis spinosa (Montagu, 1808) |
vag |
ZB |
● |
C, E |
|
Tanystylum orbiculare Wilson, 1878 Clase Thecostraca Orden Balanomorfa |
vag |
ZB |
●, C, E |
C, E |
|
Chthamalus fragilis Darwin, 1854 |
ses |
ZA, ZB |
● |
F |
|
Megabalanus tintinnabulum (Linnaeus, 1758) |
ses |
ZA, ZB |
● |
F |
|
Tetraclita stalactifera (Lamarck, 1818) Clase Malacostraca Orden Amphipoda |
ses |
ZA, ZB |
● |
F, H, I, L |
|
Corophiidae |
vag |
ZB |
● |
|
|
Categorías taxonómicas |
FC/MO |
Zonación |
Espigones y referencias en el litoral de Tuxpan |
Referencias en litoral de Veracruz |
|
Gammaridae |
vag |
ZB |
● |
|
|
Caprella sp. Orden Decapoda |
vag |
ZB |
● |
|
|
Acanthonyx petiverii H. Milne Edwards, 1834 |
vag |
ZB |
● |
I, L |
|
Arenaeus cribrarius (Lamarck, 1818) |
vag |
ZB, PM |
● |
D, H, I |
|
Calcinus tibicen (Herbst, 1791) |
vag |
ZB, PM |
● |
D, F |
|
Callinectes sp. |
vag |
ZB |
● |
|
|
Clibanarius antillensis Stimpson, 1859 |
vag |
ZB, PM |
● |
H, I |
|
Eriphia gonagra (Fabricius, 1781) |
vag |
ZB, PM |
● |
D, H, I |
|
Eurypanopeus sp. |
vag |
ZB, PM |
● |
|
|
Grapsus grapsus (Linnaeus, 1758) |
vag |
ZA, ZB |
● |
H, I |
|
Lysmata wurdemanni (Gibbes, 1850) |
vag |
ZB, PM |
● |
|
|
Menippe nodifrons Stimpson, 1859 |
vag |
ZA, ZB |
● |
F, I |
|
Pachygrapsus transversus (Gibbes, 1850) |
vag |
ZA |
● |
D, F, H, I, L |
|
Panulirus argus (Latreille, 1804) |
vag |
ZB |
● |
|
|
Petrolisthes armatus (Gibbes, 1850) |
vag |
ZB, PM |
● |
D |
|
Pilumnus dasypodus Kingsley, 1879 |
vag |
ZB, PM |
● |
F |
|
Plagusia depressa (Fabricius, 1775) FILO BRYOZOA Clase Gymnolaemata Orden Cheilostomatida |
vag |
ZA |
● |
D, F, H, I |
|
Biflustra cf. savartii (Audouin, 1826) |
incr |
ZB |
● |
|
|
Licornia cf. regularis (Osburn, 1940) |
arbo |
ZB |
● |
|
|
Thalamoporella floridana Osburn, 1940 FILO ECHINODERMATA Clase Echinoidea Orden Camarodonta |
masi |
ZB |
●, P |
|
|
Echinometra lucunter (Linnaeus, 1758) |
vag |
ZB, PM |
● |
H, I, L |
|
Ophiothrix sp. Clase Holothuroidea Orden Holothuriida |
vag |
ZB, PM |
● |
|
|
Holothuria (Halodeima) grisea Selenka, 1867 FILO CHORDATA Clase Ascidiacea Orden Stolidobranchia |
vag |
ZB, PM |
● |
I, L |
|
Botrylloides sp. |
incr |
ZB |
● |
|
Orden Aplousobranchia
Referencias: A= Wiley et al. (1982); B= Winston (1982); C= Child (1992); D= Álvarez et al. (1999); E= Munilla (2002); F= Hernández et al. (2010); G= González-Gándara et al. (2012); H= Vassallo et al. (2014); I= De la Cruz-Francisco et al. (2017b); J= Colín-García et al. (2018); K= Chávez-López (2020); L= Rodríguez-Muñoz et al. (2023); M= De la Cruz-Francisco (2025a); N= De la Cruz-Francisco (2025b); O= De la Cruz-Francisco (2025c); P= De la Cruz-Francisco y Sandoval-Cruz (2025).
DISCUSIÓN
|
Categorías taxonómicas |
FC/MO |
Zonación |
Espigones y referencias en el litoral de Tuxpan |
Referencias en litoral de Veracruz |
|
Didemnum sp. |
incr |
ZB |
● |
|
|
Eudistoma cf. carolinense Van Name, 1945 |
incr |
ZB |
● |
|
|
Clase Teleostei Orden Acanthuriformes Acanthurus tractus Poey, 1860 |
vag |
ZB, PM |
● |
G |
|
Chaetodon ocellatus Bloch, 1787 |
vag |
ZB, PM |
● |
G |
|
Orden Blenniiformes Abudefduf saxatilis (Linnaeus, 1758) |
vag |
ZB, PM |
● |
G, I, L |
|
Abudefduf taurus (Müller & Troschel, 1848) |
vag |
ZB, PM |
● |
G, I, L |
|
Labrisomus nuchipinnis (Quoy & Gaimard, 1824) |
vag |
ZB, PM |
● |
G, I |
|
Scartella cristata (Linnaeus, 1758) |
vag |
ZB, PM |
● |
G, I |
|
Stegastes adustus (Troschel, 1865) |
vag |
ZB, PM |
● |
G, I, L |
|
Orden Labriformes Halichoeres bivittatus (Bloch, 1791) |
vag |
ZB, PM |
● |
G |
En este estudio se identificaron 43 especies de algas bentónicas que habitan en los espigones de Tuxpan, de las cuales 24 constituyen nuevos registros locales, ya que no habían sido documentadas previamente por García-López et al. (2017) y Mateo-Cid et al. (2024), quienes reportaron un total de 53 especies para las escolleras. Con estos hallazgos, la riqueza de algas bentónicas para el litoral de Tuxpan asciende a 77 especies, lo cual representa el 19.7% de las 391 especies registradas en todo el litoral de Veracruz, región que es considerada como una de las áreas con alta diversidad ficológica en el golfo de México (Mateo-Cid et al., 2024).
La mayoría de las algas bentónicas registradas fueron epilíticas, lo que evidencia su capacidad de establecerse tanto en sustratos naturales como artificiales. Esta composición de algas bentónicas es propia del litoral de Veracruz, donde se ha documentado previamente en diferentes localidades, y ocupan sustratos rocosos naturales como arenisca y roca volcánica, así como también en escolleras (Arvizu-Coyotzi, 2019; De la Cruz-Francisco et al., 2017b; GarcíaGarcía et al., 2020, 2021; García-López et al., 2017; Huerta-Múzquiz, 1960; Mateo-Cid et al., 2024; Rodríguez-Muñoz et al., 2023; Sánchez-Rodríguez, 1980; Vargas-Hernández & RamírezRodríguez, 2006). Además, varios de los conjuntos de algas observadas en los espigones, tienen presencia en los arrecifes coralinos del suroeste del golfo de México (De la Cruz-Francisco et al., 2020; Galicia-García & Morales-García, 2007).
Al comparar la riqueza de algas de este hábitat artificial con otras regiones de Veracruz, se observa que varias localidades presentan mayor número de especies en comparación al litoral de Tuxpan (Mateo-Cid et al., 2024). Estas diferencias se pueden atribuir a las características del sustrato, por ejemplo, en Barra de Cazones existe una amplia plataforma de sustrato rocoso natural de tipo arenisca, con pasto marino y pozas de marea, lo que favorece el establecimiento de más especies (De la Cruz-Francisco et al., 2017b; Mateo-Cid et al., 2024). Por el contrario, los espigones del litoral de Tuxpan son estructuras pequeñas, estrechas, y aisladas predominando el sustrato arenoso, donde las rocas son angulosas, factores que limitan el establecimiento de algas marinas.
En cuanto a la zonación, el ensamblaje de algas que habitan en los espigones presentó un patrón de zonación vertical similar al de los litorales rocosos naturales. Los géneros de algas más diversos en especies se ubicaron en la zona alta y también tuvieron presencia en la cresta de la zona baja. Normalmente este tipo de algas bentónicas son típicas del intermareal medio y alto, y soportan la desecación (Rodríguez-Muñoz et al., 2023). Esta riqueza de especies de Cladophora y Cualerpa también se han reportado para otras localidades de Veracruz (De la Cruz-Francisco et al., 2017b; García-López et al., 2017; Mateo-Cid et al., 2024). En cambio, para las zonas bajas influenciadas por la marea, se registró mayor riqueza de especies y se observó un mayor desarrollo de comunidades de algas rojas, formando densos matorrales sobre los costados de los espigones. Estos contrastes en la riqueza coinciden con lo documentado para litorales rocosos de la región (De la cruz-Francisco et al., 2017b; Rodríguez-Muñoz et al., 2023). Sin embargo, se sugiere que futuros estudios evalúen cuantitativamente la riqueza, cobertura y biomasa de estas comunidades considerando el patrón de zonación vertical, las temporadas climáticas (lluvias, nortes, secas), el impacto de las actividades humanas y contaminación, así como el uso de técnicas moleculares para obtener una identificación taxonómica más precisa (García-García et al., 2021; García-López et al., 2017; Mateo-Cid et al., 2024).
En relación a la fauna, los espigones proporcionan un sustrato estable que favorece el asentamiento de diversas comunidades faunísticas, sin embargo, la riqueza faunística registrada fue menor en comparación con otros ecosistemas naturales de la región (De la Cruz-Francisco et al., 2017b; Vassallo et al., 2014). Esta diferencia puede atribuirse a las características físicas del sustrato, dado que los espigones, son cortos, estrechos y establecidos en un litoral arenoso, mientras que los litorales rocosos naturales son más extensos, heterogéneos y proveen mayor disponibilidad de recursos, por lo que suelen ser más diversos en especies al proveer mayor número de microhábitats (Firth et al., 2013). Por lo tanto, aunque los espigones sirven de sustrato para múltiples especies marinas, su menor heterogeneidad estructural limita la disponibilidad de hábitats y se ve reflejada en una riqueza faunística inferior a la documentada en ecosistemas naturales (De la Cruz-Francisco et al., 2017b; Vassallo et al., 2014). Esto demuestra que la capacidad de estas estructuras artificiales para funcionar como hábitats marinos es limitada en comparación con los sustratos rocosos naturales (Aguilera et al., 2014; Lawrence et al., 2021).
Entre los aportes más relevantes de este estudio fue la adición de dos especies de briozoos como nuevos registros para el suroeste del golfo de México, región que cuenta con pocos reportes de especies en comparación a otras zonas del golfo (Winston & Maturo, 2009). Se identificó a Biflustra cf. savartii, una especie incrustante común que se observó cubriendo la superficie de las rocas en la zona baja de los espigones y cohabitando con esponjas incrustantes como Timea hechteli y Placospongia ruetzleri. Los ejemplares revisados concuerdan con la descripción de Winston (1982), quien lo reportó como Membranipora savartii para las costas de Florida. Asimismo, se identificó a Licornia cf. regularis, un briozoo arborescente reportado como Scrupocellaria regularis en Florida (Winston, 1982), y originalmente descrito en Puerto Rico (Osburn, 1940). Por lo anterior, se extiende el rango de distribución de estas especies al suroeste del golfo de México, sumándose al reciente reporte del briozoo masivo Thalamoporella floridana (De la Cruz-Francisco & Sandoval-Cruz, 2025).
Asimismo, se reporta por primera vez para esta región a Pennaria disticha, un hidrozoo colonial y arborescente, observado frecuentemente en las pozas de marea y que puede confundirse con macroalgas erectas. Esta especie ha sido previamente reportada en el norte de golfo de México (Calder & Cairns, 2009), por lo que su hallazgo en este estudio amplía su distribución al suroeste del Golfo. Respecto al grupo de los picnogónidos, se adicionan tres nuevos registros (Ammothella appendiculata, Endeis spinosa, y Anoplodactylus californicus), de los cuales A. appendiculata representa un nuevo registro para el suroeste del Golfo, ya que previamente solo se había reportado para las costas de Texas (Child, 1992; Ramírez-Tello et al., 2022). Con estos registros, se incrementan a seis especies de picnogónidos para el litoral de Tuxpan, Veracruz.
También, se extiende la distribución del poliqueto tubícola Phragmatopoma caudata hacia el norte de Veracruz, ya que anteriormente se había reportado desde el centro de Veracruz hasta Brasil (Chávez-López, 2020). Esta especie construye estructuras biogénicas sobre sustratos rocosos, las cuales son relevantes al proporcionar microhábitats para diversos invertebrados y peces (Santos-Mella et al., 2017). En este estudio, las formaciones biogénicas se observaron principalmente a los costados y en la cresta de los espigones, especialmente en la zona alta.
Cabe mencionar que se registraron dos especies exóticas. La primera corresponde al bivalvo exótico Electroma vexillum, nativo del Indo-Pacifico, fue encontrado en la zona baja de los espigones asociada a macroalgas. Esta especie previamente fue documentada por primera vez en el litoral rocoso de Cazones en 2018 y posteriormente en los espigones de Tuxpan (2023-2024), donde se reportaron agregaciones densas sobre varias especies de macroalgas rojas y verdes (De la Cruz-Francisco, 2025c). Asimismo, la presencia de E. vexillum ha sido documentada recientemente en Brasil (2022–2023) en ambientes intermareales y submareales, asociada a macroalgas y pastos marinos (Rocha-Barreira et al., 2025). En este estudio se confirma nuevamente su presencia en los espigones de Tuxpan, habitando en los talos de algas rojas y algas verdes, lo que refuerza la evidencia de su establecimiento en el golfo de México. La segunda especie exótica corresponde al coral exótico Oculina patagonica, del cual se observaron colonias incrustantes desde el 2021. Esta especie fue reportada inicialmente en el sur de Veracruz (González-Gándara et al., 2015a) y su identidad taxonómica se confirmó mediante análisis moleculares con especímenes colectados en arrecifes del puerto de Veracruz (ColínGarcía et al., 2018). Posteriormente, su presencia fue registrada en el litoral rocoso de Cazones (De la Cruz-Francisco et al., 2017b; Rodríguez-Muñoz et al., 2023).
Por lo tanto, los espigones pueden actuar como vectores que facilitan el asentamiento de especies exóticas e invasoras, lo cual es preocupante dado que a solo 15 km de la costa se encuentran arrecifes coralinos. De hecho, en la región ya se han establecido al menos dos peces exóticos: Pterois spp., y Neopomacentrus cyanomos (De la Cruz-Francisco et al., 2015; González-Gándara et al., 2012; 2015b). Debido a lo anterior, es prioritario implementar estrategias de prevención, monitoreo y manejo ante la presencia de especies exóticas tanto en la zona litoral de los espigones y escolleras.
Por otra parte, la composición de la fauna vágil integrada principalmente por gasterópodos, picnogónidos, crustáceos, poliquetos, equinodermos y peces, coincide con comunidades intermareales descritas para ecosistemas rocosos naturales de Veracruz (Álvarez et al., 1999; Arvizu-Coyotzi, 2019; De la Cruz-Francisco et al., 2017b; Hernández et al., 2010; HernándezÁlvarez & Álvarez, 2007; Rodríguez-Muñoz et al., 2023; Quintana & Molina, 1991; VargasHernández & Ramírez-Rodríguez, 2006; Wiley et al., 1982). Así mismo, el ensamblaje de especies sedentarias (anémonas y balanos) registradas en este estudio también es característico de las zonas intermareales rocosas y de los arrecifes coralinos de la región (De la Cruz-Francisco et al., 2017b; Quintana & Molina, 1991; Rodríguez-Muñoz et al., 2023; Wiley et al., 1982).
Respecto a la comunidad faunística sésil, también se observó un patrón de zonación vertical, concentrándose en las zonas bajas de los espigones y en las pozas de marea, la cual es común en ecosistemas naturales del litoral de Veracruz (De la Cruz-Francisco et al., 2017b; Quintana & Molina, 1991; Rodríguez-Muñoz et al., 2023). Esta comunidad estuvo representada principalmente por formas incrustantes y masivas de esponjas, corales y briozoos, una morfología típica para tolerar el impacto del oleaje (Calder & Cairns, 2009; van Soest, 2017; Winston, 1982; Winston & Maturo, 2009). Sin embargo, parte de la composición de esponjas parece ser única en este hábitat artificial (con excepción de Cinachyrella alloclada y Placospongia ruetzleri), ya que las especies identificadas recientemente para el área de estudio (De la Cruz-Francisco, 2025a) no se han documentado en los ecosistemas naturales o en los arrecifes cercanos de la región, donde ya se han realizado inventarios previos (De la Cruz-Francisco et al., 2017b; De la Cruz-Francisco & Bandala-Pérez, 2016; Gómez & Heras-Escutia, 2022).
Con relación a los ensamblajes faunísticos (poliquetos, gasterópodos, anfípodos, decápodos y picnogónidos) asociados en varias especies de algas verdes (Ulva, Chaetomorpha y Caulerpa) y rojas (Gracilaria, Hypnea, Acantophora, Padina), se atribuye a que las macroalgas proporcionan protección, alimento y sitios de reproducción (Aguilera & De la Cruz-Francisco, 2017; Guerra-García et al., 2011; Vicente et al., 2024). Sin embargo, estas asociaciones han sido poco documentadas en la región (Aguilera & De la Cruz-Francisco, 2017). Actualmente, con la presencia del bivalvo exótico E. vexillum colonizando estas macroalgas representa una amenaza para este ensamblaje nativo (De la Cruz-Francisco, 2025c), por lo que es imprescindible evaluar posibles impactos sobre la estructura de las comunidades de algas e invertebrados, tal como ha sido sugerido para las costas de Brasil (Rocha-Barreira et al., 2025).
En cuanto a la identificación taxonómica, parte del ensamblaje faunístico asociado a las algas fue identificado a nivel de especie o género para los grupos de gasterópodos, decápodos y picnogónidos, cuyas especies ya han sido previamente registradas en ecosistemas naturales de la región (Álvarez et al., 1999; De la Cruz-Francisco et al., 2017b; García-Cubas & Reguero, 2004; Hermoso-Salazar et al., 2019; Child, 1992; Hernández et al., 2010; Vargas-Hernández & Ramírez-Rodríguez, 2006; Vassallo et al., 2014). En cambio, anfípodos, poliquetos y ascidias solo fueron identificados hasta nivel de familia y/o género, debido a la complejidad morfológica que caracteriza estos grupos taxonómicos. Por lo que es indispensable la colaboración con especialistas de cada grupo biológico y utilizar herramientas complementarias como los análisis moleculares, con la finalidad de obtener identificaciones más precisas. Estas estrategias permitirán validar la presencia de especies nativas y detectar oportunamente la presencia de especies exóticas o invasoras en estos hábitats artificiales, así también contribuirá a elaborar inventarios más completos, reduciendo los vacíos de conocimiento que aún persisten en varios grupos taxonómicos.
Finalmente, este estudio incrementa el conocimiento sobre la biodiversidad marina presente en los espigones de Tuxpan, Veracruz, y demuestra que estas estructuras artificiales son relevantes dentro del litoral que es principalmente arenoso, al proporcionar un sustrato estable para diversas comunidades marinas compuestas en su mayoría por especies representativas de los ecosistemas naturales de la región. Sin embargo, el registro de dos especies exóticas evidencia que los espigones también pueden actuar como sitios potenciales para el establecimiento y dispersión de especies no nativas hacia los ecosistemas naturales cercanos, como los arrecifes coralinos o lagunas costeras. Por lo que es importante desarrollar estrategias de monitoreo, manejo y conservación de las especies nativas, así como promover acciones de prevención, detección y control de especies exóticas a fin de evitar impactos negativos en los ecosistemas naturales de la región.
AGRADECIMIENTOS
El autor agradece a Flor Teresa Sosa Hernández, Ana Patricia Aparicio Lucas, Salvador Rodríguez Muñoz, Richard Eduardo Mandujano Solís, Diana Citlali Priante Trejo y Sheyla Stefany Hernández Perea, quienes brindaron su apoyo en los muestreos de campo. A los revisores anónimos por sus comentarios y sugerencias.
REFERENCIAS
Abele, L. G., & Kim, W. (1986). An Illustrated Guide to the Marine Decapod Crustaceans of Florida. Parte 1 Technical Series, 8(1), 1–326.
Aguilera, M. A., Broitman, B. R., & Thiel, M. (2014). Spatial variability in community composition on a granite breakwater versus natural rocky shores: lack of microhabitats supprress intertidal biodiversity. Marine Pollution Bulletin. 87, 257–268. http://dx.doi.org/10.1016/j.marpolbul.2014.07.046">http://dx.doi. http://dx.doi.org/10.1016/j.marpolbul.2014.07.046">org/10.1016/j.marpolbul.2014.07.046
Aguilera-Pérez, A. E. & De la Cruz-Francisco, V. (2017). Composición taxonómica de las algas césped y su macrofauna asociada, arrecife Tuxpan, Sistema Arrecifal Lobos-Tuxpan. Boletín del Instituto Oceanográfico de Venezuela, 56(2), 66–80.
Álvarez, F., Villalobos, J. L., Rojas, Y., & Robles, R. (1999). Listas y comentarios sobre los crustáceos decápodos de Veracruz, México. Anales del Instituto de Biología Universidad Nacional Autónoma de México, Serie Zoología, 70(1), 1–127.
Arvizu-Coyotzi, J. K. (2019). Caracterización macrobentónica de la zona litoral entre punta Gorda a Antón Lizardo, Veracruz. [Tesis de Maestría. Universidad Veracruzana].
Borrero, P., Benavides, G. H., & Díaz S. C. M. (2012). Equinodermo del Caribe Colombiano II: Echinoidea y Holothuroidea. Series de publicaciones especiales del Invermar No. 30. Santa Marta, 250 pp.
Bulleri, F., & Chapman, M. G. (2004) Intertidal assemblages on artificial and natural habitats in marinas on the north-west coast of Italy. Marine Biology, 145, 381–391.
Calder, D. R., & Cairns, S. D. (2009). Hydroids (Cnidaria: Hydrozoa) of the Gulf of Mexico. In Felder, D. L. & Camp, D. K. (eds). Gulf of Mexico, Origin, Water, and Biota. Biodiversity (pp. 381–394). Texas A & M University Press, College Station, Texas.
Celis, A., Rodríguez-Almaráz, G., & Álvarez, F. (2007). Los cirripedios torácicos (Crustacea) de aguas someras de Tamaulipas, México. Revista Mexicana de Biodiversidad, 78(2), 325– 337.
Chávez-López, Y. (2020). New species and new records of Phragmatopoma (Polychaeta:
Sabellariidae) from Tropical America. Zootaxa, 4845(3), 301–330. https://doi.org/10.11646/zootaxa.4845.3.1
Child, C. A. (1992). Shallow water Pycnogonida of the Gulf of Mexico. Florida Marine Research Institute, Memories of he Hourglass Cruises, 9(1), 1–86.
Colín-Garcia, N. A., Campo, J. E., Tello-Musi, J. L., Pérez-España, H., & Carrara, X. C. (2018). First record of the invasive coral Oculina ptagonica de Angelis, 1908 (Cnidaria, Scleractinian) in the Gulf of Mexico. Check List, 14(4), 613–617. https://doi.org/10.15560/14.4.613
De la Cruz-Francisco, V. (2025a). Esponjas marinas (Porifera: Demospongiae) de los espigones de Tuxpan, Veracruz, con nuevos registros para México. Novitates Caribaea, (25), 1–20.
https://doi.org/10.33800/nc.vi25.366
De la Cruz-Francisco, V. (2025b). Nuevas adiciones de babosas marinas (Gastropoda: Heterobranchia) para el norte de Veracruz y sur del golfo de México. Novitates Caribaea, (25), 32–53. https://doi.org/10.33800/nc.vi25.368
De la Cruz-Francisco, V. (2025c). First record of the Indo-Pacific species Electroma vexillum (Bivalvia: Pteriidae) in the Gulf of Mexico. Ciencias Marinas, 51. https://doi.org/10.7773/cm.y2025.3528
De la Cruz-Francisco, V., & Bandala-Pérez, A. E. (2016). Esponjas y Cnidarios (Hydrozoa y Anthozoa) del arrecife Oro Verde; cobertura bentónica afinidad faunística con ecosistemas arrecifales de Veracruz, México. CICIMAR Oceánides, 31(2), 45–64. https://doi.org/10.37543/oceanides.v31i2.185
De la Cruz-Francisco, V., & González-Gándara, C. (2006). Lista actualizada de los gasterópodos de la planicie del Arrecife Lobos, Veracruz, México. UDO Agrícola, 6(1), 128–137.
De la Cruz-Francisco, V., González-González, M. &, Morales-Quijano, I. (2015). Ampliación del ámbito de distribución geográfica de la especie exótica: Neopomacentrus cyanomos (Bleeker, 1856) (Perciformes-Pomacentridae) en el Sistema Arrecifal Lobos-Tuxpan, Veracruz, México. Revista Investigaciones Marinas, 35, 101–108.
De la Cruz-Francisco V., González-González, M., & Morales-Quijano, I. (2016a). Faunística y distribución de Demospongiae: Porífera del arrecife Enmedio, Sistema Arrecifal LobosTuxpan, México. CICIMAR Oceánides, 31(1), 7–16. https://doi.org/10.37543/oceanides.v31i1.155
De la Cruz-Francisco V., González-González, M., & Morales-Quijano, I. (2016b). Inventario taxonómico de Hydrozoa (Orden: Anthoathecata) y Anthozoa (Subclases: Hexacorallia y Octocorallia) del Arrecife Enmedio, Sistema Arrecifal Lobos-Tuxpan. CICIMAR Oceánides, 31(1), 23–34. https://doi.org/10.37543/oceanides.v31i1.157
De la Cruz-Francisco, V., & González-Muñoz, R. (2019). Las anémonas marinas de los sistemas arrecifales de Veracruz. En: Granados-Barba, A., Ortiz-Lozano, L., González-Gándara, C. & Salas-Monreal, D. (eds.). Estudios Científicos en el Corredor Arrecifal del Suroeste del Golfo de México (pp. 139–156). Universidad Autónoma de Campeche.
De la Cruz-Francisco, V., Hernández-Herrera, R., I., Ortigosa, D., & Cuervo-González, R. (2023). Updated list and new records of sea slugs (Gastropoda: Heterobranchia) in the Lobos-Tuxpan Reef System, Mexico. Hidrobiológica, 33(1), 39–50.
De la Cruz-Francisco V., Morales-Quijano, I., & González-González, M. (2017a). Equinodermos del polígono arrecifal Tuxpan, Área de Protección de Flora y Fauna, México. Revista Investigaciones Marinas, 37(2), 46–60.
De la Cruz-Francisco, V., & Sandoval-Cruz, D. E. (2025). Primer registro de Thalamoporella floridana Osburn, 1940 (Bryozoa: Cheilostomatida) en el suroeste del golfo de México. Revista Ciencias Marinas y Costeras, 17(2), 55–65. https://doi.org/10.15359/revmar.17-2-3
De la Cruz-Francisco, V., Orduña-Medrano, R. E., & González-González, M. (2020). Lista actualizada de la flora marina bentónica de cinco arrecifes coralinos del norte de Veracruz, México. Revista Ciencias Marinas y Costeras, 12(1), 69–97. https://doi.org/10.15359/revmar.12-1.4
De la Cruz-Francisco, V., Orduña-Medrano, R. E., Paredes-Flores, J. E., Vázquez-Estrada, R. I., González-González, M., & Flores-Galicia, L. (2017b). Una aproximación a la florística y faunística de la costa rocosa El Pulpo, Cazones, Veracruz, México. CICIMAR Oceánides, 32(1), 39–58. https://doi.org/10.37543/oceanides.v32i1.195
De la Cruz-Francisco, V., Ortigosa, D., & González-González, M. (2017c). Primeros registros de babosas marinas (Gastropoda: Heterobranchia) del Sistema Arrecifal Tuxpan, México, con ampliaciones de ámbito de distribución. Biodiversity and Natural History, 3(1), 15–23.
Díaz, M.C., Pomponi, S. A., & Van Soest, R. W. M. (1993) A systematic revision of the central West Atlantic Halichondrida (Demospongiae, Porifera). Part III: Description of valid species. In: Uriz, M.-J. & Rützler, K. (Eds.), Recent Advances in Ecology and Systematics of Sponges. Scientia Marina, 57(4), 283–306.
Dreckman, K. M. (2012). Los géneros Gracilaria e Hydropuntia (Gracilariaceae, Rhodophyta) en las costas mexicanas del Golfo de México. Monografías Ficológicas, 4,111–204.
Dreckmann, K. M., & Pérez-Hernández, M. A. (1994). Macroalgas bentónicas de la laguna de Tampamachoco, Veracruz, México. Revista de Biología Tropical, 43(3), 715–717.
Firth, L., B., Thompson, R. C., White, F. J., Schofield, M., Skov, M. W., Hoggart, S. P. G., Jackson, H. J., Knights, A. M., & Hawkins, S. J. (2013). The importance of water-retaining features for biodiversity on artificial intertidal coastal defence structures. Diversity and distributions, 19(10), 1275–1283. https://doi.org/10.1111/ddi.12079
Flores-Galicia, L., & De la Cruz-Francisco, V. (2018). Primeros registros de medusas (Cubozoa, Scyphozoa), sifonóforos (Hydrozoa) y ctenóforos (Tentaculata) del sistema arrecifal LobosTuxpan, México. CICIMAR Oceánides, 33(1), 25–38. https://doi.org/10.37543/oceanides.v33i1.222
Galicia-García, C., & Morales-García, A. (2007). Investigaciones sobre macroalgas realizadas en el Sistema Arrecifal Veracruzano. En: Granados-Barba, A., Abarca-Arenas, L. G. & VargasHernández, J. M. (eds). Investigaciones Científicas en el Sistema Arrecifal Veracruzano (pp. 141–160). Universidad Autónoma de Campeche.
García-Cubas, A., & Reguero, M. (2004). Catálogo ilustrado de Moluscos Gasterópodos del Golfo de México y Mar Caribe. Universidad Nacional Autónoma de México.
García-Cubas, A., & Reguero, M. (2007). Catálogo ilustrado de Moluscos Bivalvos del Golfo de México y Mar Caribe. Universidad Nacional Autónoma de México.
García-García, A. M. E., Cabrera-Becerril, E., Núñez-Resendiz, M. L., Dreckmann, K. M., & Senties, A. (2020). Actualización taxonómica de las algas rojas (Rhodophyta) marinas bentónicas del Atlántico mexicano. Acta Botanica Mexicana. 127, e1677. https://doi.org/10.21829/abm127.2020.1677
García-García, A. M. E., Cabrera-Becerril, E., Núñez-Resendiz, M. L., Dreckmann, K. M., & Sentíes, A. (2021). Actualización taxonómica de las algas pardas (Phaeophyceae, Ochrophyta) marinas bentónicas del Atlántico mexicano. Acta Botanica Mexicana. 128, e1968. https://doi.org/10.21829/abm128.2021.1968
García-López, D. Y., Mateo-Cid, L. E., & Mendoza-González, A. A. (2017). Nuevos registros y lista actualizada de las algas verdes (Chlorophyta) del litoral de Veracruz, México. Gayan Botanica, 74(1): 41–56. https://doi.org/10.4067/s071766432017005000104
Gómez, P., & Heras-Escutia, N. (2022). Porifera (Demospongiae) con nuevos registros para México. En: Hernández-Aguilera, J. L. & Arenas-Fuentes, V. (eds.) Ecología y el Antropoceno en el Arrecife: un elemento del complejo arrecifal veracruzano (pp. 115–147). Universidad Veracruzana, México.
González-Gándara, C., De la Cruz-Francisco, V., Salas-Pérez, J. J., & Domínguez-Barradas, C. (2012). Lista de los peces de Tuxpan, Veracruz, México. UDO Agrícola, 12(3), 675–689.
González-Gándara, C., Domínguez-Barradas, C., De la Cruz-Francisco, V., Solís-Marín, F. A., & Carricart-Ganivet, J. P. (2015a). Esponjas, corales escleractinios, equinodermos y peces de arrecifes coralinos del norte y sur de Veracruz. Universidad Veracruzana. Informe final SNIB-CONABIO, proyecto No. JF124. México, D.F.
González-Gándara, C., Solís-Marín, F. A., De la Cruz-Francisco, V., Granados-Barba, A., SalasPérez, J. J., & Argüelles-Jiménez, J. (2015b). Riqueza y distribución de equinodermos en los arrecifes del norte y sur de Veracruz, México. Revista de Biología Tropical, 63(Suppl. 2), 183–193.
Guerra-García, J. M., Cabezas, M., Baeza-Rojano, E., Izquierdo, D., Corzo, J., Ros, M., Sánchez, J. A., Dugo-Cota, A., Flores-León, A. M., & Soler-Hurtado, M. M. (2011). Abundance patterns of macrofauna associated to marine macroalgae along the Iberian Peninsula. Zoologica Baetica, 22, 3–17.
Hall, A. E., Herbert, R. J. H., Britton, J. R., & Hull, S. L. (2018). Ecological enhancement techniques to improve habitat heterogeneity on coastal defence structures. Estuarine, Coastal and Shelf Science. 210, 68–78. https://doi.org/10.1016/j.ecss.2018.05.025
Hermoso-Salazar, M., Arvizu-Coyotzi, K., & Ayón-Parente, M. (2019). Riqueza de especies de crustáceos malacostracos de los sistemas arrecifales Lobos-Tuxpan y Veracruzano. En: Granados-Barba, A., Ortiz-Lozano, L., González-Gándara, C. & Salas-Monreal, D. (eds). Estudios Científicos en el Corredor Arrecifal del Suroeste del Golfo de México (pp. 113– 138). Universidad Autónoma de Campeche.
Hernández, C., Álvarez, F., & Villalobos, J. L. (2010). Crustáceos asociados a sustrato duro en la zona intermareal de Montepío, Veracruz, México. Revista Mexicana de Biodiversidad, 81, S141-S151.
Hernández-Álvarez, C., & Álvarez, F. (2007). Changes in the crustacean community of a tropical rocky intertidal shore: is there a pattern? Hidrobiologica, 17(1), 25-34.
Huerta-Múzquiz, L. (1960). Lista preliminar de las algas marinas del estado de Veracruz. Boletín de la Sociedad Botánica de México, 25, 39–45.
Humann, P., & Deloach, N. 2002. Reef fish identification Florida, Caribbean, Bahamas. Jacksonville, Florida: New Publications.
Landa-Cansigno, C. L., Mateo-Cid, L. E., Mendoza-González, A. C., & Guerrero-Analco, J. A. (2019). Macroalgas marinas del litoral rocoso Neovolcánico de Veracruz, México. Acta Botanica Mexicana, 126, e1525. https://doi.org/10.21829/abm126.2019.1525
Lawrence, P. J., Evans, A. J., Jackson-Bué, T., Brooks, P. R., Crowe, T. P., Dozier, A. E., Jenkis, S. R., Moore, P. J., Williams, G. J., & Davies, A. J. (2021). Artificial shorelines lack natural structural complexity across scales. Proceedings of the Royal Society B, 288, 1951.
https://doi.org/10.1098/rspb.2021.0329
León-Álvarez, D., Candelaria-Silva, C., Hernández-Almaráz, P., & León-Tejera, H. (2007). Géneros de algas marinas tropicales de México: I. Algas Verdes. Ed. Las prensas de Ciencias, Facultad de Ciencias, UNAM, 173 pp.
Littler, D. S., & Littler, M. M. (2000). Caribbean Reef Plants. An Identification Guide to the Reef Plants of the Caribbean, Bahamas, Florida and Gulf of México. Offshore Graphics. Washington. 542 pp.
López-Portillo, J., Moreno-Casasola, P., Silva R, Martínez, M. L., Jiménez-Orocio, O., Chávez, V., Mendoza-González, G., Cruz, C., Vázquez, G., Lithgow, D., García-Franco, J. G., & Castillo-Campos, G. (2023). La zona costera del municipio Tuxpan, Veracruz. México: INECOL, Veracruz, 80 pp.
López-Torres, C. K., Mendoza-Becerril, M. A., & De la Cruz-Francisco, V. (2023). Medusozoans of Tuxpan, Veracruz, Gulf of Mexico. Regional Studies in Marine Science, 63, 102987. https://doi.org/10.1016/j.rsma.2023.102987
Masi, B. P., Macedo, I. M. & Zalmon, I. R. (2009). Benthic community zonation in a breakwater on the North coast of the State of Rio de Janeiro, Brazil. Brazilian Archives of Biology and Technology, 52(3), 637–646.
Mateo-Cid, L. E., Mendoza-González, A. C., García-López, D. Y., Hernández-Casas, C. M. & Méndez-Guzmán, I. (2024). Diversidad de algas marinas bentónicas del litoral de Veracruz, México. Acta Botanica Mexicana, 131, e2316. https://doi.org/10.21829/abm131.2024.2316
Mendelssohn, I. A., Byrnes, M. R., Kneib, R. T., & Vittor, B. A. (2017). Coastal habitats of the Gulf of Mexico. In: H Ward (ed), Habitats and biota of the Gulf of Mexico: before the deepwater horizon oil spill (pp. 359–640). New York (USA): Springer.
Mendoza-González, C. A., Mateo-Cid, L. E., García-López, D. Y., & Acosta-Calderón, J. A. (2014). Diversity and distribution of articulated Coraline algae (Rhodophyta, Corallinales) of the Atlanctic coast of Mexico. Phytotaxa, 190,1, 045–063. http://dx.doi.org/10.11646/phytotaxa.190.1.6">http://dx.doi.org/10.11646/phytotaxa.190.1.6
Mineur, F., Cook, E. J, Minchin, D., Bohn, K., MacLeod, A., & Maggs, C. A. (2012). Changing coasts: marine aliens and artificial structures. Oceanography and Marin Biology: An Annual Review, 50, 189–234.
Miranda-Alves, A., Nacimento-Moura, C. W. D. N., Limoeiro-Alves, G., & De Souza Gestinari, L. M. (2009). Os gêneros Chaetomorpha Kütz. nom. cons. e Rhizoclonium Kütz. (Chlorophyta) do litoral do Estado da Bahia, Brasil. Revista Brasileira de Botânica, 32(3), 545–570.
Morales-Quijano, I., De la Cruz-Francisco, V., González-González, M., & Argüelles-Jiménez, J. (2017). Diversidad y abundancia de los equinodermos y su relación con la cobertura bentónica del arrecife Enmedio, Sistema Arrecifal Lobos-Tuxpan, México. Revista Ciencias Marinas y Costeras, 9(2), 51–74. https://doi.org/10.15359/revmar.9-2.3
Munilla, T. (2002). Pycnogonida. En: Llorente, J. & Morrone, J. (eds.). Biodiversidad, taxonomía y biogeografía de artrópodos de México: Hacia una síntesis de su conocimiento (pp. 215–
222). Vol. III, Comisión para el Conocimiento y Uso de la Biodiversidad, México
Oliveira, L. de M., Gamba, G. A. & Moreira da Rocha, R. (2014). Eudistoma (Ascidiacea:
Polycitoridae) from tropical Brazil. Zoologia, 31(2), 195–208.
http://dx.doi.org/10.1590/S1984-46702014000200011">http://dx.doi.org/10.1590/S1984-46702014000200011
Ortiz-Lozano, L., Arceo-Briseño, P., Granados-Barba, A., Salas-Monreal, D., & JiménezBadillo, L. (2010). Zona costera. En: G. Benítez & Rodríguez, W. (eds.), Atlas del Patrimonio Natural, histórico y Cultural de Veracruz (pp. 123–146). Tomo 1 Patrimonio Natural, México.
Osburn, R. C. (1940). Bryozoa of Porto Rico with a resume of West Indian Bryozoan fauna. Scientific Survey of Porto Rico and Virgin Islands, 16, 321–486.
Pacheco-Cervera, M. C., Pacheco-Ruíz, I., Ramos-Miranda, J., Cetz-Navarro, N. P., & SotoÁvila, J. L. (2010). Presencia del género Caulerpa en la Bahía de Campeche, Camp. Hidrobiológica, 20(1), 57–69.
Quintana y Molina, J. (1991). Resultados del programa de Investigaciones en Arrecife Veracruzanos del Laboratorio de Sistemas Bentónicos Litorales. Hidrobiológica, 1(1), 73– 86
Quiroz-González, N., León-Álvarez, D., & Rivas-Acuña, M. G. (2017). Nuevos registros de algas verdes marinas (Ulvophyceae) para Tabasco, México. Acta Botanica Mexicana, 118, 121–138. https://doi.org/10.21829/abm118.2017.1204
Ramírez-Tello, L. M., Tello-Musi, J. L., & López-García, R. (2022). Pycnogonida de aguas mexicanas: listado con observaciones en diversidad y ecología. Boletín de Investigaciones Marinas y Costeras, 51(1), 151–170. https://doi.org/10.25268/bimc.invemar.2022.51.1.1186
Reguero, M., García-Cubas, A., & Zúñiga, G. (1991). Moluscos de la laguna de Tampamachoco, Veracruz, México: Sistemática y Ecología. Anales del Instituto de Ciencias del Mar y Limnología, 18(2), 289–328.
Rocha-Barreira, C. A., da Silva, E. J., Oliver, P. G., Carvalho, R., Menezes, F. M., & Brito, L. (2025). The exotic Bivalve Electroma vexillum (Reeve, 1857) (Bivalvia: Vulsellidae) on the Brazilian coast. Arquivos de Ciências do Mar, Fortaleza, 28(1),10–21. https://doi.org/10.36517/acmar.v58i1.95522
Rodríguez-Muñoz, S., Granados-Vargas, N., & De la Cruz-Francisco, V. (2023). Análisis de la comunidad vágil y sésil del intermareal rocoso de Cazones, Veracruz, México. Novitates Caribaea, (22), 25–50. https://doi.org/10.33800/nc.vi22.337
Román-Hernández, U., Valdez Z., J., & Zavala G., F. (2006). Composición y abundancia del ictioplancton durante la temporada de estiaje en la laguna de Tampamachoco, Veracruz, México. Revista UDO Agrícola, 6(1), 138–149.
Salas-Pérez, J. J., Ocaña-Valencia, A. N., & González-Gándara, C. (2015). Temperatura superficial del mar y concentración de clorofila-a en zonas arrecifales y desembocadura de sus ríos en el Golfo de México occidental. En: Granados-Barba, A., Ortiz-Lozano, L. D. & González-Gándara, C. (eds.), Aportes al conocimiento del Sistema Arrecifal Veracruzano: hacia el corredor arrecifal del suroeste del Golfo de México (pp. 315–332). Universidad Autónoma de Campeche.
Sánchez-Rodríguez, M. E. (1980). Ficoflora del sustrato rocoso dentro de las costas del Golfo de México, México. Boletim do Instituto Oceanográfico, 29(2), 347–350.
Santos-Mella, F., Contreras-Puigbó, A., Pugibet, E., & Rivas, D. V. (2017). Ecología y biodiversidad de un arrecife formado por Phragmatopoma caudata Kroyer in Mörch (Canalipalpata: Sabellariidae) en República Dominicana. Novitates Caribaea, (11), 69–78.
https://doi.org/10.33800/nc.v0i11.16
van Soest, R. W. M. (2017). Sponges of the Guyana Shelf. Zootaxa, 4217(1), 001–225. https://doi.org/10.11646/zootaxa.4217.1.1
Vargas-Hernández, J. M., & Ramírez-Rodríguez, A. (2006). Los arrecifes rocosos. En: MorenoCasasola, P. (ed.), Entornos veracruzanos: la costa de La Mancha (pp. 381–403). Instituto de Ecología, A. C., Xalapa, Ver. México.
Vaselli, S., Bulleri, F., & Benedetti-Cecchi, L. (2008). Hard coastal-defence structures as habitats for native and exotic rocky-bottom species. Marine Environmental Research, 66, 395–403. http://dx.doi.org/10.1016/j.marenvres.2008.06.002">http://dx.doi.org/10.1016/j.marenvres.2008.06.002
Vassallo, A., Dávila, Y., Luviano, N., Deneb-Amozurritia, S., Vital, X. G., Conejeros, C. A., Vázquez, L., & Álvarez, G. (2014). Inventario de invertebrados de la zona rocosa intermareal de Montepío, Veracruz, México. Revista Mexicana de Biodiversidad, 85, 349–362.
Vicente, V. S., Longo, P. A. S., Mansur, K. F. R., Serrano, H., Batistão, A. R., & Leite, F. P. P. (2024). Biodiversity of macroalgae-associated invertebrates in the marine protected area of Alcatrazes archipelago, southeastern Brazil. Biota Neotropica, 24(2), e20241610.
https://doi.org/10.1590/1676-0611-BN-2024-1610
Vieira, L. M., Almeida, A. C. S., & Winston, J. E. (2016). Taxonomy of intertidal cheilostome Bryozoa of Maceió, northeastern Brazil. Part 1: Suborders Inovicellina, Malacostegina and Thalamoporellina. Zootaxa, 4097(1), 59–83. http://doi.org/10.11646/zootaxa.4097.1.3
Wiley, G. N., Circé, R. C., & Tunnell, J. W. (1982). Mollusca of the rocky shores of east central Veracruz state, Mexico. The Nautilus, 96(2), 55–61.
Winston, J. E., & Maturo, Jr. F. J. (2009). Bryozoans (Ectoprocta) of the Gulf of Mexico. In D. L. Felder & D. K. Camp (eds.). Gulf of Mexico-Origins, Waters, and Biota Biodiversity (pp. 1147–1164). EE. UU: Texas A&M Press, College Station, Texas.
Winston, J. E. (1982). Marine bryozoans (Ectoprocta) of the Indian river area (Florida). Bulletin of the American Museum of Natural History, 173, 99–176.
Zavala-Hidalgo, J., Morey, S. L., & O’Brien, J. J. (2003). Seasonal circulation on the western shelf of the gulf of Mexico using a high-resolution numerical model. Journal of Geophysical Research: Oceans, 108(C12). http://dx.doi.org/10.1029/2003JC001879">http://dx.doi.org/10.1029/2003JC001879http://dx.doi.org/10.1029/2003JC001879">.
Zea, S., & De Weerdt, W. (1999). Haliclona (Haliclona) epiphytica n. sp. (Porifera, Demospongiae, Haplosclerida), a seaweed-dwelling sponge from the Colombian Caribbean. Beaufortia, 49(13), 171–176.
Cómo citar: De la Cruz-Francisco, V. (2026). Lista taxonómica de la biota marina asociada a los espigones del litoral de Tuxpan, Veracruz, México. Novitates Caribaea, (27), 18–44.